

I filosofi greci del V secolo a.C. diedero le risposte più disparate e fantasiose alla
questione fondamentale riguardante il principio di tutta la realtà fisica:
Per Talete il principio universale è l'acqua, per Anassimene l'aria.
Per Empedocle di Agrigento sono quattro i principi fondamentali: l'acqua, l'aria, la terra ed il fuoco.
Per Anassagora di Clazomene, fondatore della prima scuola filosofica ateniese, tutti i
corpi sono fatti di semi (per Aristotele omeomerie = parti simili), di natura diversa a
seconda della sostanza (metalli,pietre,materia vivente) e divisibili in parti sempre più
piccole (infinitesime).
I primi a parlare di atomi (dal greco atomos = indivisibile) furono
Leucippo di Mileto e Democrito di Abdera, sostenitori della discontinuità della materia.
La teoria atomica di Leucippo e Democrito, contrapposta alla divisibilità continua dei
semi di Anassagora, considera gli atomi che cadono nel vuoto per effetto del loro peso e
si aggregano formando i corpi.
Dopo oltre 2200 anni, all'inizio del XIX secolo, il chimico e fisico inglese John Dalton,
studiando le leggi delle combinazioni chimiche, dimostrò la necessità di riprendere la teoria
atomica per spiegare i rapporti ponderali costanti tra le quantità degli elementi che formano i vari composti chimici.
Gli studi di Dalton furono successivamente approfonditi dal chimico e fisico torinese
Amedeo Avogadro (1776-1856) e dal chimico palermitano Stanislao Cannizzaro (1826-1910),
che fondarono la chimica teorica moderna, fornendo solide basi per lo straordinario
sviluppo delle conoscenze fisico-chimiche del XX secolo.
Ebbe così inizio lo sviluppo della fisica atomica, che verso la fine del XIX secolo
ricevette un impulso decisivo dagli studi sui raggi catodici e sui raggi X.
La prima, chiara e decisiva conferma sperimentale della natura corpuscolare della materia fu ottenuta nel 1897 da J.J. Thomson a seguito della scoperta dell'elettrone.
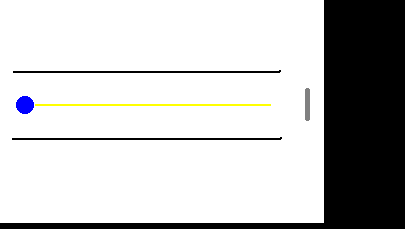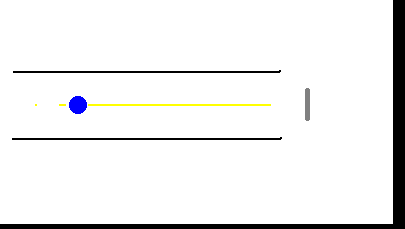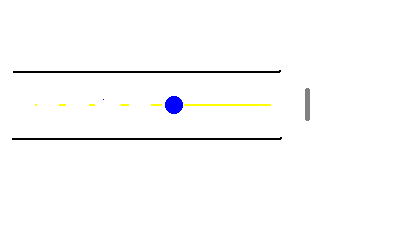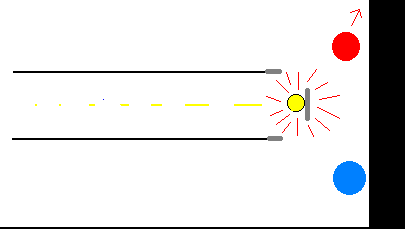
L'esplorazione del micromondo ebbe inizio nella seconda metà del
XIX secolo con lo studio della scarica elettrica nei gas rarefatti.
Erano già disponibili dispositivi di laboratorio,noti come rocchetti di
Ruhmkorff, capaci di generare alte tensioni,
dell' ordine di parecchie decine di
kV, sfruttando i fenomeni d'induzione elettromagnetica scoperti da Faraday.
Era
pertanto molto agevole studiare le caratteristiche della scarica elettrica nei
tubi (di Crookes) contenenti gas rarefatti (alla pressione di qualche
decimillesimo di mm di mercurio), e parecchi fisici si dedicarono allo studio
delle caratteristiche dei cosiddetti "raggi catodici", emessi dal catodo dei
tubi a scarica.
Nel corso di tali ricerche furono accertate le proprietà dei
"raggi catodici" di sviluppare calore nell'urto contro placchette metalliche
disposte sulla loro traiettoria all'interno dei tubi, e di essere deviati sia da
campi elettrici,applicati ai tubi (di Braun) attraverso coppie di placchette
metalliche, sia da campi magnetici generati da magneti o da elettromagneti posti
in prossimità dei tubi.
Venne inoltre accertata la proprietà di tali "raggi" di
propagarsi in linea retta dal catodo all'anodo,in assenza di campi elettrici e
magnetici, e di produrre una fluorescenza verdastra nell'impatto contro il vetro
del tubo.
Studiando sperimentalmente i raggi catodici, il fisico tedesco Roentgen (Nobel
1901) (università di Karlsruhe) ,scoprì un nuovo tipo di raggi, da lui
denominati X per la loro natura misteriosa, prodotti dalla decelerazione
subita dalle particelle catodiche nell'urto contro il vetro del tubo.
Si sa
infatti dalla teoria dell'elettromagnetismo che una carica elettrica che subisca
un'accelerazione o una decelerazione, irradia onde elettromagnetiche.
I raggi X
non essendo deviati, a differenza dei "raggi catodici",nè da campi elettrici ,
nè da campi magnetici, sono appunto, come fu accertato con diverse esperienze ,
radiazioni elettromagnetiche con lunghezza d'onda compresa tra qualche
miliardesimo di centimetro e qualche centomilionesimo di centimetro.
Roentgen
scoprì per caso i raggi X osservando la fluorescenza da essi indotta nei sali di
bario, ed osservò inoltre la loro caratteristica più importante, quella di
impressionare la lastra fotografica.
Il fisico francese Becquerel (Nobel 1903) scoprì la radioattività naturale,
avendo osservato la proprietà dei sali di uranio di impressionare la lastra
fotografica .
Scopri' in particolare,sperimentando in presenza di un campo
magnetico, che i sali di uranio emettono tre tipi di radiazioni :
a,b,g ; le
prime due di natura corpuscolare, l'ultima di natura ondulatoria.
Negli anni
immediatamente successivi altri fisici scoprirono che le particelle
a sono
dotate di carica positiva , mentre quelle
b sono cariche negativamente.
Si accertò inoltre che la radiazione g,
capace di attraversare strati di piombo
di notevole spessore, è costituita da onde elettromagnetiche caratterizzate da
una lunghezza d'onda molto minore di quella dei raggi X.
Ai coniugi Pierre e
Maria Curie ,ai quali fu conferito il premio Nobel assieme a Becquerel, si deve
la scoperta di un elemento,il radio, dotato di una radioattività molto più
intensa di quella dell'uranio, dal quale deriva per decadimento radioattivo,
attraverso una serie di elementi il cui capostipite è appunto l'uranio .
Si
scoprì inoltre che gli elementi radioattivi contenuti nelle rocce della crosta
terrestre appartengono a tre serie naturali di decadimento radioattivo,aventi
per elementi capostipiti l'uranio, il torio e l'attinio e per elementi finali
isotopi del piombo.
In altri termini, nell'arco dei 4,5 miliardi di anni di età
della Terra,dagli elementi capostipiti di ciascuna serie, per emissione di
particelle radioattive e di radiazione g si sono formati ,
in condizioni di equilibrio, tutti i successivi elementi,fino al piombo.
Infatti, determinando le
attuali concentrazioni dei vari elementi nelle rocce e misurando la velocità di
decadimento di ciascun elemento, si risale all'età della Terra.
Tra le fondamentali scoperte fisiche che caratterizzano gli ultimi anni del
XIX secolo, ricordiamo la misura del rapporto tra la carica elettrica e la massa
dei "raggi catodici",effettuata nel 1897 dal fisico inglese Joseph John Thomson
(Nobel 1906),che accertò definitivamente la loro natura corpuscolare,coniando
il termine "elettrone" per la prima particella fondamentale emessa dagli atomi
che formano la materia.
"Gli atomi sono analoghi a microscopici sistemi
planetari".
E' questa una frase molto usata per spiegare con un'analogia la
struttura dell'atomo,paragonando il Sole al nucleo atomico, la cui massa è quasi
uguale a quella dell'intero atomo , ed i pianeti in orbita intorno al Sole agli
elettroni che ruotano intorno al nucleo.
Si sa che il nucleo contiene particelle
fondamentali dette collettivamente nucleoni,cioè protoni e neutroni: i primi
circa 1840 volte più pesanti degli elettroni e dotati di carica elettrica
positiva, i secondi aventi una massa quasi uguale a quella dei protoni e privi
di carica elettrica.
Gli elettroni che orbitano intorno al nucleo ,dotati di una
carica elettrica negativa uguale in modulo a quella del protone, formano la
"corteccia" degli atomi e determinano,attraverso le forze elettromagnetiche, le
proprietà meccaniche, termiche,chimiche ed elettromagnetiche della materia
(metalli, semiconduttori e metalloidi) nei vari stati di aggregazione
(solido,liquido, gassoso).
In termodinamica si definisce corpo nero un corpo ideale capace di assorbire
tutta la radiazione termica incidente su di esso e, viceversa, di emettere con la
massima efficienza, tutta la radiazione termica corrispondente alla sua temperatura assoluta (in gradi
Kelvin).
Un corpo nero in pratica si realizza con un involucro con la superficie
interna riflettente,mantenuto a temperatura costante ed avente un forellino
attraverso il quale venga emessa o assorbita la radiazione termica (radiazione
infrarossa), il cui spettro continuo può essere esaminato con speciali
spettroscopi dotati di lenti e prismi atti a trasmettere la radiazione
infrarossa, e di sensori all'infrarosso che forniscono un segnale elettrico di
ampiezza proporzionale all'intensità della radiazione.
Un problema
teorico di notevole importanza, verso la fine del secolo XIX, era quello di
fornire una legge che riuscisse a rappresentare l'andamento delle curve
sperimentali osservate.
Parecchi fisici ,tra i quali Rayleigh, Jeans e Wien
svilupparono teorie incomplete, basate sull'elettromagnetismo classico e sulla
termodinamica,ma nessuno di loro riuscì a trovare la soluzione teorica completa
e definitiva.
Nel 1900 una soluzione innovativa fu fornita dal fisico tedesco
Max Planck (Nobel 1918), considerato per questo il padre della teoria dei
quanta: Planck ipotizzò per la prima volta la quantizzazione dell'energia
elettromagnetica associata agli oscillatori armonici (cariche elettriche dotate
di moto oscillatorio armonico) .
In particolare,impostò il calcolo del potere
emissivo del corpo nero ad una data temperatura T, considerando l'energia
assorbita o emessa da ciascun oscillatore armonico, multipla di una quantità
elementare E = h f,
essendo f la frequenza
dell'onda elettromagnetica emessa o assorbita ed h una costante universale,
nota come costante di PlancK.
La sola
introduzione di questa ipotesi bastò a Planck per risolvere definitivamente il
problema del corpo nero, fornendo le formule in grado di rendere conto delle
curve ottenute sperimentalmente.
Furono poste in tal modo le premesse teoriche
per lo sviluppo di una nuova fisica, la fisica quantistica.